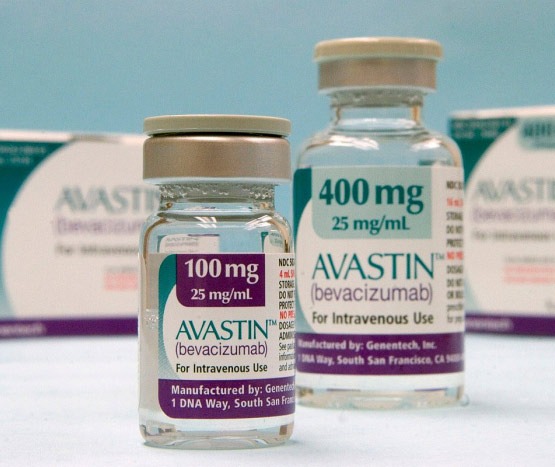
Лечение препаратом Авастин ® можно проводить только под наблюдением врача, имеющего опыт применения противоопухолевой терапии.
У пациентов, получающих Авастин ®, существует повышенный риск развития перфорации желудочно-кишечного тракта и желчного пузыря. Наблюдались тяжелые случаи перфорации ЖКТ (у менее 1% пациентов с метастатическим раком молочной железы или неплоскоклеточным немелкоклеточным раком легкого и у 2% пациентов с метастатическим колоректальным, метастатическим почечно-клеточным раком или у пациенток с раком яичников, получавших Авастин® в первой линии терапии), в том числе и фатальные (у 0.2%-1% всех пациентов, получавших Авастин®, что составляет 1/3 всех тяжелых случаев). Также наблюдались случаи перфорации ЖКТ и у пациентов с рецидивирующей глиобластомой. Клиническая картина перфораций ЖКТ отличалась по тяжести и варьировала от признаков свободного газа при рентгенографии брюшной полости, которые исчезали без лечения, до перфораций с абсцессом брюшной полости и летальным исходом. В некоторых случаях имело место исходное внутрибрюшинное воспаление в результате язвенной болезни желудка, некроза опухоли, дивертикулита или колита, ассоциированного с химиотерапией. Связь между развитием внутрибрюшинного воспаления и перфораций ЖКТ и терапией препаратом Авастин® не установлена. При развитии перфорации ЖКТ лечение препаратом Авастин® следует прекратить.
У пациентов, получающих Авастин®, существует повышенный риск образования свищей.
При терапии препаратом Авастин® зарегистрированы серьезные случаи образования свищей, включая случаи с летальным исходом. Свищи ЖКТ чаще всего возникали у пациентов с метастатическим колоректальным раком (до 2% пациентов), реже при других локализациях опухоли. Нечасто (>0.1%-<1%) регистрировались случаи образования свищей других локализаций (бронхоплевральные, урогенитальные, билиарные) при применении препарата Авастин® по различным показаниям. Случаи образования свищей регистрировались и при постмаркетинговых наблюдениях. Образование свищей чаще наблюдается в первые 6 месяцев терапии препаратом Авастин®, но может возникать как через 1 неделю, так и через 1 год и позже после начала терапии.
При возникновении трахео-эзофагеального свища или свища любой локализации 4 степени тяжести терапию препаратом Авастин® следует отменить. Существуют ограниченные сведения о продолжении использования препарата Авастин® у пациентов со свищами других локализаций. При возникновении внутреннего свища, не проникающего в ЖКТ, следует рассмотреть вопрос об отмене препарата Авастин®.
У пациентов, получающих Авастин®, повышен риск возникновения кровотечений, особенно связанных с опухолью. Авастин® следует отменить при возникновении кровотечения 3 или 4 степени тяжести по классификации NCI-CTC. Общая частота возникновения кровотечений 3-5 степени тяжести при применении препарата Авастин® по всем показаниям составляет 0.4%-5.0% по сравнению с 0-2.9% при химиотерапии. Чаще всего кровотечения были связаны с опухолью (см. ниже) или были небольшими слизисто-кожными (например, носовое кровотечение).
Слизисто-кожные кровотечения наблюдались у 50% пациентов, получавших Авастин®. Чаще всего наблюдались носовые кровотечения 1 степени тяжести по классификации NCI-CTC, длившиеся менее 5 минут, разрешившиеся без медицинского вмешательства и не требовавшие изменения режима дозирования препарата Авастин®. Частота небольших слизисто-кожных кровотечений (например, носового кровотечения) зависит от дозы препарата. Реже возникали небольшая кровоточивость десен или вагинальные кровотечения.
Кровотечения, связанные с опухолью: обильные или массивные легочные кровотечения/кровохарканье наблюдались в основном при немелкоклеточном раке легкого. Прием противоревматических/противовоспалительных препаратов, антикоагулянтов, предшествующая лучевая терапия, атеросклероз, центральное расположение опухоли, образование каверны до или во время лечения являются возможными факторами риска развития легочных кровотечений/кровохарканья, при этом только для плоскоклеточного рака легкого установлена статистически достоверная связь с развитием кровотечений. Риск развития легочных кровотечений/кровохарканья у пациентов с определенно установленным плоскоклеточным гистологическим типом опухоли или преимущественно плоскоклеточным гистологическим типом опухоли неизвестен.
У 9% пациентов с немелкоклеточным раком легкого, кроме преимущественно плоскоклеточного гистологического типа опухоли, и получавших Авастин® в комбинации с химио-терапией, наблюдались геморрагические явления любой степени тяжести по сравнению с 5% пациентов, получавших только химиотерапию. Явления 3-5 степени тяжести наблюдались у 2.3% пациентов, получавших Авастин® в комбинации с химиотерапией, и у менее 1% пациентов, получавших только химиотерапию. Обильные или массивные легочные кровотечения/кровохарканье могут возникать внезапно, а 2/3 серьезных случаев заканчиваются летальным исходом.
У пациентов с немелкоклеточным раком легкого, получающих препарат Авастин®, существует повышенный риск образования серьезных легочных кровотечений/кровохарканья, в некоторых случаях с фатальным исходом. Пациенты, недавно имевшие кровотечение/кровохарканье (более 2.5 мл крови), не должны получать Авастин®.
У пациентов с колоректальным раком возможны кровотечения ЖКТ, связанные с опухолью, в том числе ректальное кровотечение и мелена.
Редко наблюдались кровотечения при других типах опухолей и включали случаи кровотечения в ЦНС у пациентов с метастатическим поражением ЦНС и у пациентов с глиобластомой.
Частота возникновения кровотечений в ЦНС у пациентов с нелеченными метастазами в ЦНС, получавшими Авастин®, подробно не изучалась. В настоящее время имеются сведения о том, что у 3 из 91 (3.3%) пациентов с опухолями различной локализации и метастазами в ЦНС возникли кровотечения в ЦНС 4 степени тяжести при терапии бевацизумабом. У 1 из 96 (1%) пациентов, не получавших бевацизумаб, развилось кровотечение в ЦНС 5 степени тяжести. При анализе данных, полученных от 83 пациентов с лечеными метастазами в ЦНС, зарегистрирован 1 случай кровотечения в ЦНС 2 степени тяжести (1.2%).
У пациентов с рецидивирующей глиобластомой могут возникать внутричерепные кровотечения. Кровотечения в ЦНС 1 степени тяжести зарегистрированы у 2.4% (2/84) пациентов, получавших монотерапию препаратом Авастин®. Кровотечения в ЦНС 1, 2 и 4 степени тяжести зарегистрированы у 3.8% (3/79) пациентов, получавших Авастин® в комбинации с иринотеканом.
Необходимо проводить мониторинг симптомов кровотечений в ЦНС и отменить терапию препаратом Авастин® в случае возникновения внутричерепного кровотечения.
У пациентов с врожденным геморрагическим диатезом, приобретенной коагулопатией или получавших полную дозу антикоагулянтов по поводу тромбоэмболии, перед назначением препарата Авастин®следует соблюдать осторожность ввиду отсутствия информации о профиле безопасности препарата у таких пациентов. Не наблюдалось повышения частоты развития кровотечения 3 степени тяжести и выше у пациентов, получавших Авастин® и варфарин в полной дозе в связи с возникновением венозного тромбоза.
Тяжелые глазные инфекции после приготовления раствора для незарегистрированного интравитреального введения: сообщались отдельные случаи, а также серии случаев серьезных нежелательных явлений со стороны органа зрения (включая инфекционный эндофтальмит и другие воспалительные заболевания) после незарегистрированного интра-витреального введения препарата Авастин®, раствор которого был приготовлен из флаконов, предназначенных для внутривенного введения онкологическим пациентам. Некоторые из этих явлений привели к потере остроты зрения различной степени тяжести, включая стойкую слепоту.
У пациентов, получавших Авастин®, наблюдалась повышенная частота возникновения артериальной гипертензии всех степеней тяжести (до 34%) по сравнению с 14% у пациентов из групп контроля. По всем показаниям частота артериальной гипертензии 3-4 степени тяжести по классификации NCI-CTC составила 0.4%-17.9% в группе препарата Авастин®; 4 степени тяжести (гипертонический криз) наблюдалась у 1% пациентов из группы препарата Авастин® и у 0.2% из группы химиотерапии.
Клинические данные по безопасности позволяют предположить, что частота случаев повышения артериального давления (АД), вероятно, зависит от дозы бевацизумаба.
Авастин® может быть назначен только больным с предварительно компенсированной артериальной гипертензией с дальнейшим контролем АД. Информация о влиянии препарата Авастин® у пациентов с неконтролируемой артериальной гипертензией на момент начала терапии отсутствует. У пациентов с артериальной гипертензией, требующей лекарственной терапии, рекомендуется временно прекратить терапию препаратом Авастин® до достижения нормализации АД.
В большинстве случаев нормализация АД достигается с помощью стандартных антигипертензивных средств (ингибиторов АПФ, диуретиков и блокаторов кальциевых каналов), подобранных индивидуально для каждого больного. Отмена терапии препаратом Авастин® или госпитализация требовались редко.
Очень редко наблюдались случаи гипертензивной энцефалопатии, некоторые с летальным исходом. Риск возникновения артериальной гипертензии, ассоциированной с терапией препаратом Авастин®, не коррелирует с исходными характеристиками больного, сопутствующим заболеванием или сопутствующей терапией.
Терапию препаратом Авастин® необходимо прекратить при отсутствии нормализации АД, развитии гипертонического криза или гипертензивной энцефалопатии.
При терапии препаратом Авастин® зарегистрированы единичные случаи синдрома обратимой задней лейкоэнцефалопатии (редкое неврологическое заболевание, проявляющееся эпилептическим припадком, головной болью, психическими нарушениями, нарушением зрения, поражением зрительных центров коры головного мозга, с или без артериальной гипертензии и другими симптомами). Диагноз можно подтвердить с помощью методов визуализации головного мозга. В случае развития синдрома обратимой задней лейкоэнцефалопатии следует назначить симптоматическую терапию, тщательно контролировать АД и отменить Авастин®. Безопасность повторного назначения препарата Авастин® у таких пациентов не установлена.
При терапии препаратом Авастин® в комбинации с химиотерапией частота артериальной тромбоэмболии, включая инсульт, транзиторную ишемическую атаку и инфаркт миокарда и другие явления артериальной тромбоэмболии была выше, чем при назначении только химиотерапии. Общая частота возникновения случаев артериальной тромбоэмболии составила 3.8% по сравнению с 1.7% в группе контроля. У 0.8% пациентов, получавших Авастин® в комбинации с химиотерапией, и у 0.5% пациентов, получавших только химиотерапию, имелся летальный исход. Случаи нарушения мозгового кровообращения (включая транзиторную ишемическую атаку) сообщались у 2.3% пациентов, получавших Авастин®, и 0.5% пациентов из контрольной группы; случаи инфаркта миокарда – у 1.4% и 0.7%, соответственно.
При этом явления артериальной тромбоэмболии наблюдались у 11% (11/100) пациентов, получавших терапию препаратом Авастин®, и у 5.8% (6/104) пациентов, получавших химиотерапию в связи с метастатическим колоректальным раком.
При возникновении артериальной тромбоэмболии терапию препаратом Авастин® необходимо прекратить. Артериальная тромбоэмболия в анамнезе или возраст старше 65 лет ассоциируются с повышенным риском возникновения артериальной тромбоэмболии во время лечения препаратом Авастин®. При лечении таких пациентов необходимо проявлять осторожность.
Во время лечения препаратом Авастин® имеется повышенный риск развития венозной тромбоэмболии(легочная эмболия, тромбоз глубоких вен, тромбофлебит). Общая частота возникновения венозной тромбоэмболии (тромбоз глубоких вен и легочная эмболия) варьирует от 2.8% до 17.3% по сравнению с 3.2%-15.6% при химиотерапии.
Явления венозной тромбоэмболии 3-5 степени тяжести наблюдались у 7.8% пациентов, получавших Авастин® в комбинации с химиотерапией, по сравнению с 4.9% пациентов, получавших только химиотерапию. У пациентов, перенесших явление венозной тромбоэмболии и получающих терапию препаратом Авастин® и химиотерапию, имеется повышенный риск рецидива явления венозной тромбоэмболии, по сравнению с пациентами, получающими только химиотерапию.
Терапию препаратом Авастин® необходимо прекратить при возникновении жизнеугрожающей легочной тромбоэмболии (4 степень тяжести), а при степени тяжести <3 следует проводить тщательный мониторинг за состоянием пациента.
Застойная сердечная недостаточность (ЗСН) возникала при применении препарата Авастин® по всем показаниям, но в основном при метастатическом раке молочной железы.
Наблюдались как бессимптомное снижение фракции выброса левого желудочка, так и ЗСН, потребовавшая терапии или госпитализации.
При метастатическом раке молочной железы ЗСН 3 степени тяжести и выше наблюдалась у 3.5% пациентов, получавших Авастин® в комбинации с химиотерапией, по сравнению с 0.9% пациентов, получавших только химиотерапию. У пациентов, получавших Авастин® в комбинации с препаратами антрациклинового ряда, частота ЗСН 3 степени тяжести и выше не отличалась от имеющихся данных при терапии метастатического рака молочной железы: 2.9% в группе антрациклины + бевацизумаб и 0% в группе антрациклины + плацебо. При этом частота ЗСН любой степени тяжести не отличалась между двумя исследуемыми группами: 6.2% в группе антрациклины + бевацизумаб и 6.0% в группе антрациклины + плацебо. У большинства пациентов наблюдалось улучшение симптомов и/или фракции выброса левого желудочка при соответствующем лечении.
Данные о риске развития ЗСН у пациентов с ЗСН II-IV класса по NYHA в анамнезе отсутствуют.
В большинстве случаев ЗСН возникала у пациентов с метастатическим раком молочной железы, получавших терапию антрациклинами, лучевую терапию на область грудной клетки в анамнезе или с другими факторами риска развития ЗСН.
Необходимо проявлять осторожность при назначении препарата Авастин® пациентам с клинически значимым сердечно-сосудистым заболеванием в анамнезе, таким как ишемическая болезнь сердца или ЗСН.
У пациентов, которые не получали терапию препаратами антрациклинового ряда ранее, при применении препарата Авастин® и препаратов антрациклинового ряда не наблюдалось увеличения частоты ЗСН любой степени тяжести по сравнению с монотерапией препаратами антрациклинового ряда. ЗСН 3 степени тяжести и выше возникала несколько чаще в группе терапии препаратом Авастин® в комбинации с химиотерапией по сравнению с только химиотерапией, что соответствует и другим данным, полученным у пациентов с метастатическим раком молочной железы и не получающих сопутствующую терапию антрациклинами.
У пациентов с диффузной В-крупноклеточной лимфомой при терапии бевацизумабом и доксорубицином в кумулятивной дозе более 300 мг/м2 наблюдалось повышение числа новых случаев ЗСН. При сравнении терапии ритуксимаб/циклофосфамид/доксорубицин/винкристин/преднизолон (R-CHOP) + бевацизумаб и R-CHOP число новых случаев не отличалось, но было выше, чем наблюдавшееся ранее при терапии доксорубицином. Частота ЗСН была выше в группе R-CHOP + бевацизумаб.
Авастин® может отрицательно влиять на заживление ран. Лечение бевацизумабом следует начинать не менее чем через 28 дней после обширного хирургического вмешательства или при полном заживлении хирургической раны. При развитии во время лечения осложнений, связанных с заживлением раны, Авастин® необходимо временно отменить до полного заживления раны. Введение препарата Авастин®также необходимо временно прекратить в случае проведения планового хирургического вмешательства.
У пациентов с метастатическим колоректальным раком, перенесших обширные хирургические вмешательства за 28-60 дней до начала терапии препаратом Авастин®, повышенного риска послеоперационных кровотечений или осложнений, связанных с заживлением ран, не наблюдалось.
Повышение риска послеоперационных кровотечений или осложнений, связанных с заживлением ран, в течение 60 дней после обширных хирургических вмешательств наблюдалось только у пациентов, которые получали Авастин® во время операции. Частота возникновения варьировала от 10% (4/40) до 20% (3/15).
Осложнения, связанные с заживлением ран 3-5 степени тяжести наблюдались у 1.1% пациентов с местно рецидивирующим или метастатическим раком молочной железы, получавших Авастин®, по сравнению с 0.9% в группе контроля.
При терапии рецидивной глиобластомы частота послеоперационных осложнений, связанных с заживлением ран (расхождение краев раны после краниотомии и подтекание цереброспинальной жидкости), составила 3.6% у пациентов, получавших монотерапию препаратом Авастин®, и 1.3% у пациентов, получавших Авастин® в комбинации с иринотеканом.
Протеинурия наблюдалась у 0.7%-38% пациентов, получавших Авастин®. По степени тяжести протеинурия варьировала от транзиторного бессимптомного выявления следов белка в моче и нечасто (у 1.4% пациентов) до нефротического синдрома (протеинурия 4 степени тяжести). Протеинурия 3 степени тяжести зарегистрирована у 3.1% пациентов, получавших Авастин® по различным показаниям. Однако протеинурия 3 степени тяжести наблюдалась у 7% пациентов с распространенным и/или метастатическим почечно-клеточным раком. Протеинурия не ассоциировалась с нарушением функции почек и редко требовала отмены терапии препаратом Авастин®.
Риск развития протеинурии повышен у пациентов с артериальной гипертензией в анамнезе. Возможно, протеинурия 1 степени зависит от дозы препарата Авастин®.
При развитии протеинурии 4 степени Авастин® необходимо отменить. До начала и во время терапии препаратом Авастин® рекомендуется проводить анализ мочи на протеинурию.
В большинстве случаев при протеинурии >2 г в сутки терапия препаратом Авастин® временно приостанавливалась до снижения протеинурии <2 г в сутки.
При терапии препаратом Авастин® в комбинации с миелотоксичными режимами химиотерапии наблюдалось повышение частоты развития тяжелой нейтропении, фебрильной нейтропении или инфекций с тяжелой нейтропенией (включая случаи с летальным исходом) по сравнению с химиотерапией.
Пациенты старше 65 лет: при назначении препарата Авастин® пациентам старше 65 лет существует повышенный риск возникновения артериальной тромбоэмболии (включая развитие инсульта, транзиторной ишемической атаки, инфаркта миокарда), лейкопении 3-4 степени тяжести и тромбоцитопении, а также нейтропении (всех степеней тяжести), диареи, тошноты, головной боли и утомляемости по сравнению с пациентами <65 лет. Повышения частоты развития других побочных реакций, связанных с применением препарата Авастин® (перфорации ЖКТ, осложнения, связанные с заживлением ран, артериальная гипертензия, протеинурия, застойная сердечная недостаточность и кровотечения), у пациентов старше 65 лет по сравнению с пациентами <65 лет не отмечено.
У пациентов может наблюдаться повышенный риск развития инфузионных реакций/реакций гиперчувствительности. Существуют данные о более частом развитии анафилактических реакций и реакций анафилактоидного типа у пациентов, получавших Авастин® в комбинации с химиотерапией, по сравнению с пациентами, получавшими только химиотерапию.
В некоторых случаях частота данных реакций соответствует категории «часто» (до 5% у пациентов, получавших бевацизумаб).
Рекомендуется тщательное наблюдение за пациентом во время и после введения препарата Авастин®, что является общим правилом во время введения любого препарата, представляющего собой гуманизированное моноклональное антитело. При возникновении реакции необходимо прервать инфузию и провести соответствующие медицинские мероприятия. Систематическая премедикация не может являться гарантией отсутствия инфузионных реакций/реакций гиперчувствительности.
Мужчинам и женщинам детородного возраста во время лечения препаратом Авастин® и, как минимум, в течение 6 месяцев после окончания лечения необходимо использовать надежные методы контрацепции.
Авастин® может нарушать фертильность у женщин. Новые случаи недостаточности функции яичников (аменорея продолжительностью 3 мес. и более, уровень ФСГ>30мМЕ/мл, отрицательный тест на беременность c определением ß-ХГЧ в сыворотке) регистрировались чаще у пациенток, получавших бевацизумаб. У большинства пациенток фертильность восстанавливалась после прекращения терапии препаратом Авастин®. Отдаленные эффекты терапии препаратом Авастин® на фертильность неизвестны.
Перед назначением препарата Авастин® необходимо обсудить методы сохранения фертильности с женщинами детородного возраста.
Вскармливание грудным молоком не рекомендуется во время лечения препаратом Авастин® и, как минимум, в течение 6 месяцев после окончания терапии препаратом Авастин®.